रासायनिक अभिक्रिय : -
ऐसे परिवर्तन दिन में नए गुणों वाले पदार्थों का निर्माण होता है उसे रासायनिक अभिक्रिया कहते हैं
अभिकारक - ऐसे पदार्थ जो किसी रासायनिक अभिक्रिया में हिस्सा लेते हैं उन्हें अभिकारक कहते हैं
उत्पाद - ऐसे पदार्थ जिनका निर्माण रासायनिक अभिक्रिया में होता है उन्हें उत्पाद कहते हैं
रासायनिक समीकरण
किसी भी रसायनिक अभिक्रिया का रासायनिक समीकरण के द्वारा दर्शाया जाता है
रासायनिक समीकरण को संतुलन
द्रव्यमान संरक्षण का नियम के अनुसार किसी भी रासायनिक अभिक्रिया में द्रव्यमान का न तो निर्माण होता है न ही विनाश होता, अतः रसायनिक अभिक्रिया के पहले एवं उसके पश्चात प्रत्येक तत्वों के परमाणुओं की संख्या समान होनी चाहिए
रासायनिक अभिक्रियाओं के प्रकार
1 - संयोजन अभिक्रिया -इस अभिक्रिया में दो या दो से अधिक अभिकारक मिलकर एक उत्पाद बनाते हैं
उदाहरण - कोयले का दहन: -
C (s) + O2 (g)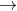 CO2 (g)
CO2 (g)
ऊष्माक्षेपी अभिक्रिया - जिन अभिक्रियाओं में उत्पाद के निर्माण के साथ-साथ उर्जा का भी उत्सर्जन होता है उसे ऊष्माक्षेपी अभिक्रिया कहते हैं
उदाहरण - प्राकृतिक गैस का दहन : -
CH4 (g) + O2 (g)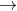 CO2 (g) + 2H2O (l) + उष्मा
CO2 (g) + 2H2O (l) + उष्मा
2 - वियोजन अभिक्रिया - जिस अभिक्रिया में एक अभिकारक टूट कर दो या दो से अधिक उत्पाद बनाते हैं उसे वियोजन अभिक्रिया कहा जाता है
वियोजन अभिक्रिया में अभिकारकों का टूटना तीन प्रकार से होता है
(i) उष्मा के द्वारा,
(ii) विद्युत के द्वारा
(iii) सूर्य की रोशनी के द्वारा
उष्मीय वियोजन - जो वियोजन उष्मा के द्वारा होता है उष्मीय वियोजन कहलाता है
उदहारण - CaCO3 (s) + उष्मा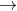 CaO (s) + CO2 (g)
CaO (s) + CO2 (g)
विद्युत वियोजन -विद्युत धारा द्वारा किया गया वियोजन विद्युत वियोजन कहलाता है
उदाहरण - 2H2O (l) + विद्युत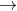 2H2 (g) + O2 (g)
2H2 (g) + O2 (g)
प्रकाशीय वियोजन - सूर्य के प्रकाश की उपस्थिति में होने वाला वियोजन प्रकाशीय वियोजन कहलाता है
उदहारण - 2AgCl (s) + सूर्य प्रकाश 2Ag (s) + Cl2
2Ag (s) + Cl2
इस अभिक्रिया का उपयोग श्याम श्वेत फोटोग्राफी में होता है
ऊष्माशोषी अभिक्रिया - जिस अभिक्रिया में अभिकारकों को तोड़ने के लिए उष्मा, प्रकाश या विद्युत की आवश्यकता होती है उसे ऊष्माशोषी अभिक्रिया कहा जाता है
उदहारण - CaCO3 (s) + उष्मा CaO (s) + CO2 (g)
CaO (s) + CO2 (g)
3 -विस्थापन अभिक्रिया - इस अभिक्रिया में अधिक क्रियाशील तत्व कम क्रियाशील तत्व को उसके यौगिक से विस्थापित कर देता है
उदहारण - CuSO4 (aq) + Zn (s) ZnSO4 (aq) + Cu (s)
ZnSO4 (aq) + Cu (s)
4 - द्विविस्थापन अभिक्रिया - जिस अभिक्रिया में उत्पादों का निर्माण, दो योगिको के बीच आयनों के आदन प्रदान से होता है उसे द्विविस्थापन अभिक्रिया कहा जाता है
उदहारण - CuSO4 (aq) + Zn (s) ⟶ ZnSO4 (aq) + Cu (s)
5 - उपचयन अपचयन
उपचयन - जब किसी पदार्थ में ऑक्सीजन की वृद्धि या हाइड्रोजन का ह्रास हो तो उसे उपचयन अभिक्रिया कहा जायेगा
उदहारण - 2Cu + O2 → 2CuO
अपचयन - जब किस अभिक्रिया में ऑक्सीजन का ह्रास हो या हाइड्रोजन की वृद्धि हो उसे अपचयन कहा जायेगा
उदहारण - CuO + Cl2 → Cu + H2O
जब उपचयन और अपचयन दोनों एक ही अभिक्रिया में हो तो उसे रेडॉक्स अभिक्रिया कहते है
दैनिक जीवन में उपचयन अभिक्रियाओ के प्रभाव
(i) संक्षारण - जब कोई धातु आद्रता, वायु, जल, अम्ल आदि के संपर्क में आता है तो धातु की उपरी परत कमजोर हो जाती है तो उसे संक्षारण कहा जाता है
उदहारण - लोहे को जंग लगना, चांदी पर कलि परत का बनना, ताम्बे पर हरी परत का बनना आदि
(ii) विकृगंधिता - वसा युक्त और तैलीय खाद्य सामग्री , वायु के संपर्क में आने पर उपचयित हो जाती है जिससे उनके स्वाद और गंध में परिवर्तन हो जाता है और वह ख़राब हो जाती है तो उसे विकृगंधिता कहा जाता है
विकृगंधिता से बचने के लिए खाद्य पैकेटो में नाइट्रोजन गैस का इस्तेमाल किया जाता है
Video lecture of this Chapter
ऐसे परिवर्तन दिन में नए गुणों वाले पदार्थों का निर्माण होता है उसे रासायनिक अभिक्रिया कहते हैं
उदाहरण - भोजन का पाचन, श्वसन, लोहे पर जंग लगना, मैग्नीशियम फीते का जलना, दही का बनना आदि
अभिकारक - ऐसे पदार्थ जो किसी रासायनिक अभिक्रिया में हिस्सा लेते हैं उन्हें अभिकारक कहते हैं
उत्पाद - ऐसे पदार्थ जिनका निर्माण रासायनिक अभिक्रिया में होता है उन्हें उत्पाद कहते हैं
रासायनिक अभिक्रिया में शामिल
अवस्था में परिवर्तन
रंग में परिवर्तन
तापमान में परिवर्तन
गैस का उत्सर्जन
रंग में परिवर्तन
तापमान में परिवर्तन
गैस का उत्सर्जन
रासायनिक समीकरण
किसी भी रसायनिक अभिक्रिया का रासायनिक समीकरण के द्वारा दर्शाया जाता है
रासायनिक समीकरण में तत्वों के प्रतिको का इस्तेमाल किया जाता है साथ ही अभिकारक और उत्पादों के रसायनिक सूत्र को उनकी भौतिक अवस्था के साथ लिखते हैं
रसायनिक अभिक्रिया में आवश्यक परिस्थितियां जैसे ताप दाब उत्प्रेरक आदि को तीर के निशान के ऊपर या नीचे दर्शाया जाता है
रासायनिक समीकरण को संतुलन
द्रव्यमान संरक्षण का नियम के अनुसार किसी भी रासायनिक अभिक्रिया में द्रव्यमान का न तो निर्माण होता है न ही विनाश होता, अतः रसायनिक अभिक्रिया के पहले एवं उसके पश्चात प्रत्येक तत्वों के परमाणुओं की संख्या समान होनी चाहिए
रासायनिक अभिक्रियाओं के प्रकार
1 - संयोजन अभिक्रिया -इस अभिक्रिया में दो या दो से अधिक अभिकारक मिलकर एक उत्पाद बनाते हैं
उदाहरण - कोयले का दहन: -
C (s) + O2 (g)
ऊष्माक्षेपी अभिक्रिया - जिन अभिक्रियाओं में उत्पाद के निर्माण के साथ-साथ उर्जा का भी उत्सर्जन होता है उसे ऊष्माक्षेपी अभिक्रिया कहते हैं
उदाहरण - प्राकृतिक गैस का दहन : -
CH4 (g) + O2 (g)
2 - वियोजन अभिक्रिया - जिस अभिक्रिया में एक अभिकारक टूट कर दो या दो से अधिक उत्पाद बनाते हैं उसे वियोजन अभिक्रिया कहा जाता है
वियोजन अभिक्रिया में अभिकारकों का टूटना तीन प्रकार से होता है
(i) उष्मा के द्वारा,
(ii) विद्युत के द्वारा
(iii) सूर्य की रोशनी के द्वारा
उष्मीय वियोजन - जो वियोजन उष्मा के द्वारा होता है उष्मीय वियोजन कहलाता है
उदहारण - CaCO3 (s) + उष्मा
विद्युत वियोजन -विद्युत धारा द्वारा किया गया वियोजन विद्युत वियोजन कहलाता है
उदाहरण - 2H2O (l) + विद्युत
प्रकाशीय वियोजन - सूर्य के प्रकाश की उपस्थिति में होने वाला वियोजन प्रकाशीय वियोजन कहलाता है
उदहारण - 2AgCl (s) + सूर्य प्रकाश
इस अभिक्रिया का उपयोग श्याम श्वेत फोटोग्राफी में होता है
ऊष्माशोषी अभिक्रिया - जिस अभिक्रिया में अभिकारकों को तोड़ने के लिए उष्मा, प्रकाश या विद्युत की आवश्यकता होती है उसे ऊष्माशोषी अभिक्रिया कहा जाता है
उदहारण - CaCO3 (s) + उष्मा
3 -विस्थापन अभिक्रिया - इस अभिक्रिया में अधिक क्रियाशील तत्व कम क्रियाशील तत्व को उसके यौगिक से विस्थापित कर देता है
उदहारण - CuSO4 (aq) + Zn (s)
4 - द्विविस्थापन अभिक्रिया - जिस अभिक्रिया में उत्पादों का निर्माण, दो योगिको के बीच आयनों के आदन प्रदान से होता है उसे द्विविस्थापन अभिक्रिया कहा जाता है
उदहारण - CuSO4 (aq) + Zn (s) ⟶ ZnSO4 (aq) + Cu (s)
5 - उपचयन अपचयन
उपचयन - जब किसी पदार्थ में ऑक्सीजन की वृद्धि या हाइड्रोजन का ह्रास हो तो उसे उपचयन अभिक्रिया कहा जायेगा
उदहारण - 2Cu + O2 → 2CuO
अपचयन - जब किस अभिक्रिया में ऑक्सीजन का ह्रास हो या हाइड्रोजन की वृद्धि हो उसे अपचयन कहा जायेगा
उदहारण - CuO + Cl2 → Cu + H2O
जब उपचयन और अपचयन दोनों एक ही अभिक्रिया में हो तो उसे रेडॉक्स अभिक्रिया कहते है
दैनिक जीवन में उपचयन अभिक्रियाओ के प्रभाव
(i) संक्षारण - जब कोई धातु आद्रता, वायु, जल, अम्ल आदि के संपर्क में आता है तो धातु की उपरी परत कमजोर हो जाती है तो उसे संक्षारण कहा जाता है
उदहारण - लोहे को जंग लगना, चांदी पर कलि परत का बनना, ताम्बे पर हरी परत का बनना आदि
(ii) विकृगंधिता - वसा युक्त और तैलीय खाद्य सामग्री , वायु के संपर्क में आने पर उपचयित हो जाती है जिससे उनके स्वाद और गंध में परिवर्तन हो जाता है और वह ख़राब हो जाती है तो उसे विकृगंधिता कहा जाता है
विकृगंधिता से बचने के लिए खाद्य पैकेटो में नाइट्रोजन गैस का इस्तेमाल किया जाता है
Video lecture of this Chapter


